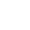Definysje fan pH-meter
In pH-meter ferwiist nei in ynstrumint dat brûkt wurdt om de pH-wearde fan in oplossing te bepalen. De pH-meter wurket neffens it prinsipe fan in galvanyske batterij. De elektromotoryske krêft tusken de twa elektroden fan 'e galvanyske batterij is basearre op 'e wet fan Nerns, dy't net allinich relatearre is oan 'e eigenskippen fan' e elektroden, mar ek relatearre is oan 'e konsintraasje fan wetterstofionen yn' e oplossing. Der is in oerienkommende relaasje tusken de elektromotoryske krêft fan 'e primêre batterij en de wetterstofionkonsintraasje, en de negative logaritme fan' e wetterstofionkonsintraasje is de pH-wearde. De pH-meter is in gewoan analytysk ynstrumint, dat in soad brûkt wurdt yn 'e lânbou, miljeubeskerming en yndustry. De pH fan 'e boaiem is ien fan' e wichtige basiseigenskippen fan 'e boaiem. Faktoaren lykas de temperatuer en ionsterkte fan 'e oplossing dy't test wurde moat, moatte wurde beskôge tidens de pH-mjitting.
It prinsipe fan in pH-meter
pH wurdt definiearre as de negative logaritme fan 'e wetterstofionkonsintraasje yn 'e wetterige oplossing. Hoewol dit yngewikkeld klinkt, is pH yn hiel ienfâldige termen in getal dat brûkt wurdt om de soerheid of alkaliniteit fan in oplossing te kwantifisearjen. It getal jout it oantal wetterstofionen oan dat in spesifike stof yn 'e oplossing frijlitte kin. Yn it pH-berik wurdt in pH fan 7 as neutraal beskôge. Oplossingen mei in pH fan 0-7 wurde as soer beskôge, en oplossingen boppe 7 oant 14 wurde alkaline oplossingen neamd. Yn biologyske systemen is pH kritysk. Mei tank oan 'e soarchfâldich oanpaste pH kinne de measte biomolekulen yn ús lichem poerbêste funksjes útfiere. Sels yn in eksperiminteel systeem moat de fereaske pH hanthavene wurde om krekte resultaten te krijen. Dêrom wurdt yn biologyske eksperiminten in apparaat mei de namme pH-meter brûkt om de pH soarchfâldich te kontrolearjen.
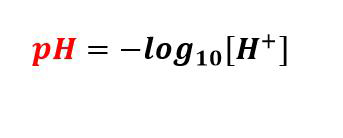
De pH-meter is in pH-responsive elektrode dy't de aktiviteit fan wetterstofionen yn in oplossing mjit en dizze ynformaasje trochstjoert. It apparaat bestiet út twa glêzen buizen, dy't elk in elektrode, in referinsje-elektrode en in sensor-elektrode befetsje. De referinsje-elektrode is makke fan in verzadigde KCl-oplossing, wylst de sensor-elektrode in bufferoplossing befettet mei in pH fan 7, en de sulveren tried bedekt mei sulverchloride is ûnderdompele yn dizze twa oplossingen. Oan 'e ein fan' e sensor-elektrode sit in bol makke fan poreus glês bedekt mei silika en metaalsâlt.
Om de pH fan 'e oplossing te mjitten, wurdt de pH-meter yn 'e oplossing ûnderdompele. Nei't de lampe fan 'e sensorelektrode yn kontakt komt mei de oplossing, sille de wetterstofionen yn 'e oplossing de metaalionen op 'e lampe ferfange. Dizze ferfanging fan metaalionen soarget derfoar dat der stroom streamt yn 'e metalen tried, dy't troch in voltmeter ôflêzen wurdt.
De pH-meter is ien fan 'e meast brûkte apparatuer yn biologyske laboratoaria. Analysearje routinematich de pH fan buffers, oplossingen en reagentia om te soargjen dat de eksperimintele omstannichheden korrekt binne. Om krekte mjittingen te garandearjen, moat de apparatuer regelmjittich kalibrearre wurde.
Tapassing fan pH-meterdetektor
Tapassing fan pH-meterdetektor yn húshâldlik rioelwettersuveringsproses

Tapassing fan pH-meter yn elektroplatearjende ôffalwettersuvering

Tapassing fan online pH-meter yn 'e yndustry

Kalibraasje fan pH-meter
Pleatsingstiid: 15 desimber 2021